Co to jest diagnostyka molekularna
Tradycyjna diagnostyka chorób alergicznych wykorzystuje testy wykrywające przeciwciała E we krwi lub skórze z użyciem ekstraktów alergenów. Ekstrakty uzyskane np. z ziaren zbóż, roztoczy kurzu domowego czy sierści kota zawierają zarówno istotne, jak i nieistotne dla reakcji alergicznej komponenty.
Co to są przeciwciała E? Jaki jest mechanizm reakcji alergicznej? Alergeny to substancje wywołujące odpowiedź immunologiczną (układu odpornościowego). Zwykle są one niegroźne dla zdrowego człowieka, ale są rozpoznawane przez układ odpornościowy osoby z nadwrażliwością jako stanowiące zagrożenie, z którym należy walczyć. Ta walka manifestuje się objawami choroby alergicznej. Swoiste przeciwciała klasy E (sIgE) są narzędziem układu odpornościowego wytwarzanym przez organizm do walki z patogenami (wirusami, bakteriami). W reakcji alergicznej, układ ten rozpoznaje np. pyłki, roztocze czy pokarmy za wroga i wytwarza te przeciwciała wobec konkretnych komponent tych alergenów. |
Obecnie istnieje możliwość stosowania w diagnostyce pojedynczych molekuł – jest to duży krok w kierunku precyzyjnej diagnostyki i lepszego prowadzenia pacjenta z choroba alergiczną.
Diagnostyka molekularna (CRD, ang. component resolved diagnostics) chorób alergicznych umożliwia analizę swoistych przeciwciał wobec ściśle określonych molekuł (komponent) wchodzącym w skład alergenu (tzw. testy mikrooznaczeń). W odniesieniu do tradycyjnej diagnostyki opartej na ekstraktach alergenowych, zwiększa czułość oznaczeń sIgE, pozwala ustalić precyzyjny profil uczuleniowy danej osoby oraz zidentyfikować molekuły reagujące krzyżowo.
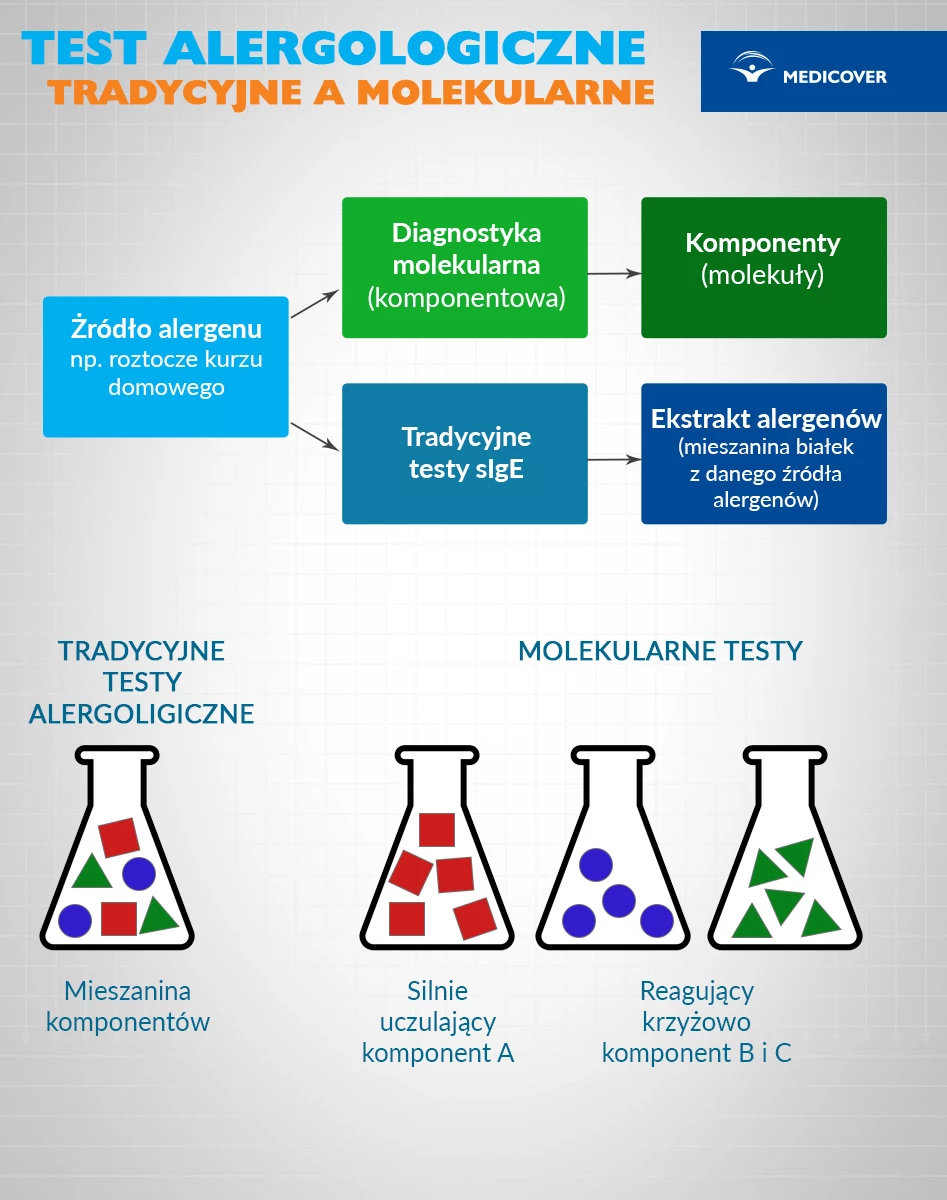
Co to jest reakcja krzyżowa, a czym uczulenie pierwotne? Niektóre alergeny zbudowane są z molekuł o podobnej budowie. Przeciwciała wytworzone przez układ odpornościowy do walki z konkretnym alergenem, w przypadku pojawienia się alergenu o podobnej budowie mogą go rozpoznać jako ten uczulający – mówimy wtedy o reakcjach krzyżowych. W poszczególnych alergenach mogą występować tzw. swoiste molekuły – czyli takie, których występowanie jest charakterystyczne tylko dla danego źródła (np. tylko w orzechu ziemnym). Diagnostyka molekularna umożliwia zatem różnicowanie alergii pierwotnej z alergią krzyżową. W przypadku molekuł reagujących krzyżowo pomaga określić, jakie inne alergeny mogą wywoływać u pacjenta objawy nadwrażliwości. Umożliwia precyzyjniejsze określenie źródeł uczulających alergenów, tym samym osoba z alergią otrzymuje ukierunkowane zalecenia dotyczące ograniczeń ekspozycji na alergeny. Testy z użyciem ekstraktów nie dają takiej możliwości. |
Zalety diagnostyki molekularnej
Diagnostyka molekularna chorób alergicznych:
- pozwala na określenie precyzyjnego profilu molekularnego choroby alergicznej;
- przy nadwrażliwości na wiele alergenów umożliwia odróżnienie uczulenia pierwotnego od objawów związanych z reakcją krzyżową;
- określa prawdopodobieństwo nabycia tolerancji;
- pomaga przewidzieć poziom nasilenia objawów choroby alergicznej;
- może zmniejszać potrzebę wykonywania prób prowokacji;
- poprawia zalecenia dotyczące eliminacji alergenu z diety;
- w alergii wziewnej identyfikuje precyzyjnie uczulające alergeny, ułatwiając dobranie odpowiedniej immunoterapii,;
- w alergii pokarmowej ocenia ryzyka anafilaksji na podstawie charakterystyki fizycznej/chemicznej istotnych alergenów;
- w alergii na lateks pomaga poprawnie zidentyfikować prawdziwie uczulonych pacjentów, którzy potrzebują eliminacji kontaktu z lateksem;
- w alergii na jad owadów błonkoskrzydłych jest niezwykle pomocna w doborze właściwej immunoterapii swoistej w rozróżnieniu nadwrażliwości na jad pszczoły i osy;
- wyższa swoistość i czułość testów molekularnych zwiększa wykrywalność uczulających alergenów.
W praktyce przekłada się to dla osoby z choroby alergiczną na:
- świadomość wysokiego ryzyka ciężkiej reakcji ogólnoustrojowej:
- co umożliwia przedsięwzięcie odpowiednich środków zapobiegawczych u osób z grupy ryzyka, czy bezwzględnego noszenia ze sobą adrenaliny;
- świadomość niskiego ryzyka reakcji ogólnoustrojowej:
- co znacząco wpływa na komfort życia osoby uczulonej – bez konieczności uporczywego czytania etykiet, sprawdzania i dopytywania o skład każdego dania ze względu na śladowe ilości różnych alergenów w potrawach;
- znajomość źródeł alergenów będących przyczyną objawów alergii i możliwość wpływu na ich bezpośrednie i pośrednie narażenie;
- monitorowanie zmian profilu uczuleń konkretnego pacjenta i prognozowanie przebiegu alergii;
- precyzyjniejsze dostosowanie zaleceń terapeutycznych;
- klasyfikację do immunoterapii (odczulania) odpowiednim alergenem;
- mniejszą liczbę wizyt i skrócenie czasu postępowania diagnostycznego.
Wyniki badań diagnostyki molekularnej
Diagnostyka molekularna stanowi w diagnostyce chorób alergicznych trzeci krok alergologów po wywiadzie i badaniach z wykorzystaniem ekstraktów (testy skórne lub sIgE z krwi).
Dodatnie wyniki testów diagnostyki molekularnej, podobnie jak testów skórnych i innych wyników z badań z krwi, są istotne tylko w przypadku współwystępowania klinicznie istotnych objawów wskazujących na reakcję alergiczną. Otrzymany dodatni wynik można jeszcze potwierdzić próbą prowokacji.
Ujemny wynik dla molekuł alergenowych i ekstraktu alergenowego z dużym prawdopodobieństwem wyklucza chorobę alergiczną.
Istnieje również strategia diagnostyczna, według której diagnozowanie choroby alergicznej rozpoczyna się od wykonania pełnego panelu diagnostyki molekularnej w pierwszym kroku diagnostycznym. Dopiero po otrzymaniu wyników takich testów przeprowadzany jest wywiad kliniczny z pacjentem, uwzględniający wyniki dodatnie dla poszczególnych molekuł alergenowych. Taki schemat diagnostyczny szczególnie sprawdza się w przypadku osób z alergią IgE-zależną, którzy uczuleni są na wiele alergenów.
Głównymi celami wykonywania diagnostyki komponentowej są:
- identyfikacja ryzyka anafilaksji u osób z alergią pokarmową,
- dobranie odpowiedniej immunoterapii (odczulania) u osób z alergią wziewną.
Interpretacja testu zawsze powinna być wykonywana przez lekarza.
| Diagnostyka molekularna pozwala na podstawie jednej próbki krwi określić profil uczulenia pacjenta, m.in.: czy jest on uczulony na jeden czy wiele alergenów i na jakie konkretnie molekuły. Badania te nie wymagają specjalnego przygotowania, np. bycia na czczo. |
Zastosowania diagnostyki molekularnej
Diagnostyka komponentowa jest stosowana w wielu sytuacjach klinicznych, m.in.:
- u osób z nadwrażliwością na wiele alergenów niezwiązanych ze sobą, np. pyłki różnych gatunków roślin lub u osób z objawami po spożyciu różnych produktów roślinnych na skutek reakcji krzyżowej;
- w przypadku przebytej ciężkiej reakcji po spożyciu pokarmów pochodzenia roślinnego i zwierzęcego;
- u osób z nadwrażliwością na wiele alergenów różnych gatunków zwierząt futerkowych;
- u osób z przebytą reakcją anafilaktyczną związaną z jadem owadów błonkoskrzydłych, zarówno pszczoły miodnej, jak i osy;
- w przypadku podejrzenia alergii na lateks.
Diagnostyka molekularna a alergia wziewna
W przypadku alergii wziewnej na wiele alergenów ważne jest, aby zidentyfikować, które molekuły alergenowe – swoiste czy też te reagująco krzyżowo – są odpowiedzialne za reakcję alergiczną. Szczególnie istotne jest to w kwalifikacji pacjenta do immunoterapii. W przypadku uczulenia na trawy czy drzewa warto pogłębić diagnostykę o molekuły alergenowe, ponieważ dodatni wynik dla swoistych molekuł traw czy drzew wiąże się z większą szansą na skuteczne odczulanie. Wskazanie swoistych uczulających molekuł pozwala precyzyjnie ustalić alergen do immunoterapii.
Dowiedz się więcej: Alergiczny nieżyt nosa – objawy, leczenie, domowe sposoby
Diagnostyka molekularna a alergia pokarmowa
W przypadku osób z alergią pokarmową, głównym zadaniem diagnostyki molekularnej jest ocena ryzyka wystąpienia wstrząsu anafilaktycznego (czyli ogólnoustrojowej reakcji alergicznej). U osób z alergią pokarmową w celu weryfikacji wpływu danego pokarmu wykonuje się próbę prowokacji. Próba prowokacji podejrzanym pokarmem jest najbardziej obiektywną metodą diagnozowania alergii pokarmowej, jednak w trakcie jej przeprowadzania może dojść do wystąpienia objawów zagrażających życiu (wstrząsu anafilaktycznego). Pogłębienie diagnostyki testem molekularnym w wielu przypadkach pozwala wskazać molekułę odpowiedzialną za objawy nadwrażliwości i odpowiedzieć na pytanie, jakie ryzyko anafilaksji niesie za sobą uczulenie na nią. W wielu przypadkach, u osób z wysokim ryzykiem anafilaksji, diagnostyka molekularna powala na rezygnację z próby prowokacyjnej.

Dokładniejsza znajomość uczulających alergenów pokarmowych wiąże się również ze wskazaniem możliwych źródeł, w których mogą być uczulające molekuły. Znajomość uczulających pokarmów, ogranicza konieczność eliminacji pokarmów według tzw. tablic reakcji krzyżowych, dzięki czemu nie trzeba wykluczać tak wielu pokarmów – w praktyce oznacza to, mniej restrykcyjną dietę eliminacyjną.
Dowiedz się więcej: Nietolerancja pokarmowa i alergia pokarmowa. Objawy i leczenie nietolerancji i alergii pokarmowych.
Diagnostyka molekularna a alergia na jad owadów
W alergii na jad owadów błonkoskrzydłych diagnostyka komponentowa jest niezwykle pomocna w doborze właściwej immunoterapii swoistej (odczulania), pozwalając na rozróżnienie nadwrażliwości na jad między pszczołą miodną a osą. Jest to szczególnie ważne, ponieważ niezmiernie trudno jest wyeliminować możliwość kontaktu latem z tymi owadami. Alergie te mogą wiązać się z ciężkimi reakcjami ogólnoustrojowymi. Diagnostyka molekularna precyzyjnie ustala, czy immunoterapia powinna odbyć się jednym wybranym jadem (pszczoły lub osy) czy obydwoma tymi alergenami.
Dowiedz się więcej: Na ratunek uczulonym na jad owadów
Diagnostyka molekularna a alergia na lateks
Diagnostyka komponentowa pozwala zidentyfikować osoby faktycznie uczulone na lateks, co minimalizuje ryzyko niepotrzebnego ograniczenia ekspozycji na ten alergen u osób bez potwierdzonej nadwrażliwości.
Diagnostyka molekularna versus tradycyjna sIgE
Diagnostyka molekularna, jak i tradycyjne testy diagnostyczne oparte na ekstraktach, są stosowane tylko w chorobach alergicznych IgE-zależnych, czyli tych przebiegających z wytwarzaniem swoistych przeciwciał klasy E, np.: w pokrzywce, anafilaksji, obrzęku naczynioruchowym, zespole alergii jamy ustnej, astmie IgE-zależnej, alergicznym nieżycie nosa, alergii pokarmowej manifestującej się objawami żołądkowo-jelitowymi.
PORÓWNANIE DIAGNOSTYKI MOLEKULARNEJ I TRADYCYJNEJ | ||
Porównywana cecha | Porównywana cecha | Porównywana cecha |
Poziom analizy | Molekuły (komponenty) | Ekstrakty alergenowe stanowiące mieszaninę uczulających i nieuczulających komponentów |
Zastosowanie | Choroby alergiczne IgE-zależne (z udziałem przeciwciał klasy E) | |
Rozróżnienie uczulenia pierwotnego od reakcji krzyżowej | Tak (np. ALEX, Polycheck) | Nie |
Ocena ryzyka wystąpienia anafilaksji | Tak | Nie |
Przewidywanie poziomu nasilenia objawów | Tak | Nie |
| Przykłady | ALEX®, FABER®, ImmunoCAP ISAC®, Polycheck® | Testy z krwi sIgE (ALEX®, FABER®, Polycheck®), punktowe testy skórne |
Opracowanie własne na podstawie [2, 4‒6].
Techniki diagnostyki molekularnej
Obecnie na rynku są dostępne różne techniki przeprowadzania diagnostyki molekularnej chorób alergicznych. Poniżej wymieniono najczęściej stosowane.
- ImmunoCAP ISAC® (the Immuno-Solid Phase Allergen Chip, Thermo Fisher) ‒ pierwszy wprowadzony kilkanaście lat temu test, który wykorzystuje do pomiaru specyficznych przeciwciał E technologię biochipu. Pozwala oznaczyć IgE wobec 112 molekuł alergenowych z 51 źródeł.
- Nowszym testem jest FABER® (the patient-Friendly Allergen nano-Bead ARray, Centri Associati di Allergologia Molecolare-CAAM) ‒ oznacza swoiste IgE wobec molekuł i ekstraktów. Jest to multiparametrowy test immunoenzymatyczny w nanotechnologii, pozwalający oznaczyć IgE wobec 244 komponentów alergenowych (122 molekuły + 122 ekstrakty alergenowe) z 123 źródeł alergenowych.
- Polycheck® (Biocheck GmBH) ‒ test immunoenzymatyczny do oznaczania sIgE wobec wybranych molekuł i ekstraktów, ułożonych w panele celowane, np. w kierunku oceny nadwrażliwości na roztocze (zawierający 2 ekstrakty roztoczy i 4 molekuły roztoczy) czy na pyłki (zawierający 2 ekstrakty – brzozy i trawy, tymotki łąkowe, oraz 6 molekuł alergenowych). Umożliwia również diagnostykę molekularną celowaną alergii pokarmowej, np. panel Polycheck® mleko plus gluten.
- ALEX® (Allergy Explorer®, MacroArray Diagnostics) oznacza swoiste przeciwciała E wobec molekuł i ekstraktów również w teście multiparametrowym immunoenzymatycznym. Obecnie pozwala na zbadanie 295 alergenów, w tym 178 molekuł i 117 ekstraktów. Analizuje alergeny pokarmowe (np. owoce, warzywa, orzechy, mleko i jaja, przyprawy), wziewne (m.in. drzewa, trawy i chwasty, zwierzęta, roztocze, pleśnie i drożdżaki), kontaktowe (drożdże i lateks) oraz jad osy i pszczeli.
Ograniczenia diagnostyki molekularnej
Z perspektywy praktyki klinicznej, wykrycie swoistych IgE oznacza uczulenie, ale warunkiem rozpoznania choroby alergicznej jest wystąpienie również objawów klinicznych. Interpretacja wyniku musi być wykonywana w kontekście wywiadu i objawów choroby alergicznej.
Brak wykrycia IgE nie wyklucza alergii, ponieważ może ona przebiegać w innym niż IgE-zależnym mechanizmie.
Kluczowe w diagnostyce choroby alergicznej są objawy kliniczne. Przesiewowe wykonywanie oznaczeń sIgE nie jest wskazane – liczba alergenów zwykle przewyższa faktyczną liczbę tych powodujących objawy kliniczne.
W wielu przypadkach nie jest konieczna aż tak precyzyjna diagnostyka.
Ograniczeniem może być również koszt badania, w większości przypadków testy wykonywane są odpłatnie.
Przeczytaj także: Testy alergiczne - kiedy i gdzie wykonać badania na alergię?
Referencje:
- Matricardi PM, Kleine-Tebbe J, Hoffmann HJ, et al. EAACI Molecular Allergology User's Guide. Pediatr Allergy Immunol. 2016;27 Suppl 23:1‐250. doi:10.1111/pai.12563
- Villalta D., Tonutti E., Bizzaro N. i wsp., Recommendations for the use of molecular diagnostics in the diagnosis of allergic disease. Ann. Allergy Clin. Immunol. 2018; 50(2): 51–58.
- Zawadzka-Krajewska A. Diagnostyka molekularna – czy jest potrzebna. Alergia 2018; 1: 15-17.
- Samoliński B., Choina M., Majsiak E. Korzyści jakie przynosi diagnostyka molekularna w rozpoznawaniu i leczeniu alergii. Alergia 2019; 1: 33-40.
- Ansotegui IJ, Melioli G, Canonica GW, et al. IgE allergy diagnostics and other relevant tests in allergy, a World Allergy Organization position paper. World Allergy Organ J. 2020;13(2):100080. Published 2020 Feb 25. doi:10.1016/j.waojou.2019.100080
- Steering Committee Authors; Review Panel Members. A WAO - ARIA - GA2LEN consensus document on molecular-based allergy diagnosis (PAMD@): Update 2020. World Allergy Organ J. 2020;13(2):100091. Published 2020 Mar 7. doi:10.1016/j.waojou.2019.100091
- Kowalski M.L., Bartuzi Z., Bręborowicz A. i wsp. Stanowisko grupy ekspertów Polskiego Towarzystwa Alergologicznego w sprawie postępowania u chorych na astmę i choroby alergiczne w okresie pandemii SARS-CoV-2. Aktualizacja 01.06.2020.
- Majsiak E., Choina M., Cukrowska B. ALEX – nowe narzędzie diagnostyczne do diagnostyki molekularnej alergii IgE-zależnej. Alergia 2019; 3: 15-18.
- Samoliński B., Raciborski F., Lipiec A. i wsp. Epidemiologia Chorób Alergicznych w Polsce (ECAP). Alergologia Polska 2014; I: 10-18.
- Kowal K. Diagnostyka molekularna alergii na roztocza kurzu domowego. Alergia 2019; 4: 23-28.
- Majsiak E. Od odkycia IgE, poprzez nanotechnologię do medycyny spersonalizowanej. Alergia 2019; 4: 41-46.
- Buczyłko K. Komponenty pyłku traw na przykładzie tymotki. Alergia 2018; 3: 17-23.
Prezentowanych informacji o charakterze medycznym nie należy traktować jako wytycznych postępowania medycznego w stosunku do każdego pacjenta. O postępowaniu medycznym, w tym o zakresie i częstotliwości badań diagnostycznych i/lub procedur terapeutycznych decyduje lekarz indywidualnie, zgodnie ze wskazaniami medycznymi, które ustala po zapoznaniu się ze stanem pacjenta. Lekarz podejmuje decyzję w porozumieniu z pacjentem. W przypadku chęci realizacji badań nieobjętych wskazaniami lekarskimi, pacjent ma możliwość ich odpłatnego wykonania. Należy potwierdzić przy zakupie badania szczegóły do jego przygotowania. |

 Medicover
Medicover




