Pragniemy poinformować, że szczepienia przeciwko COVID-19 nie są aktualnie realizowane w placówkach Medicover. Przypominamy, że najnowsze informacje na temat szczepień w ramach Narodowego Programu Szczepień przeciwko wirusowi SARS-CoV-2 dostępne są również na dedykowanej stronie: gov.pl/szczepimysie. |
Spis treści:
- Szczepienia przeciwko COVID-19
- Szczepionka na COVID-19 - kolejna dawka przypominająca
- Szczepionka na COVID-19 materiały do pobrania
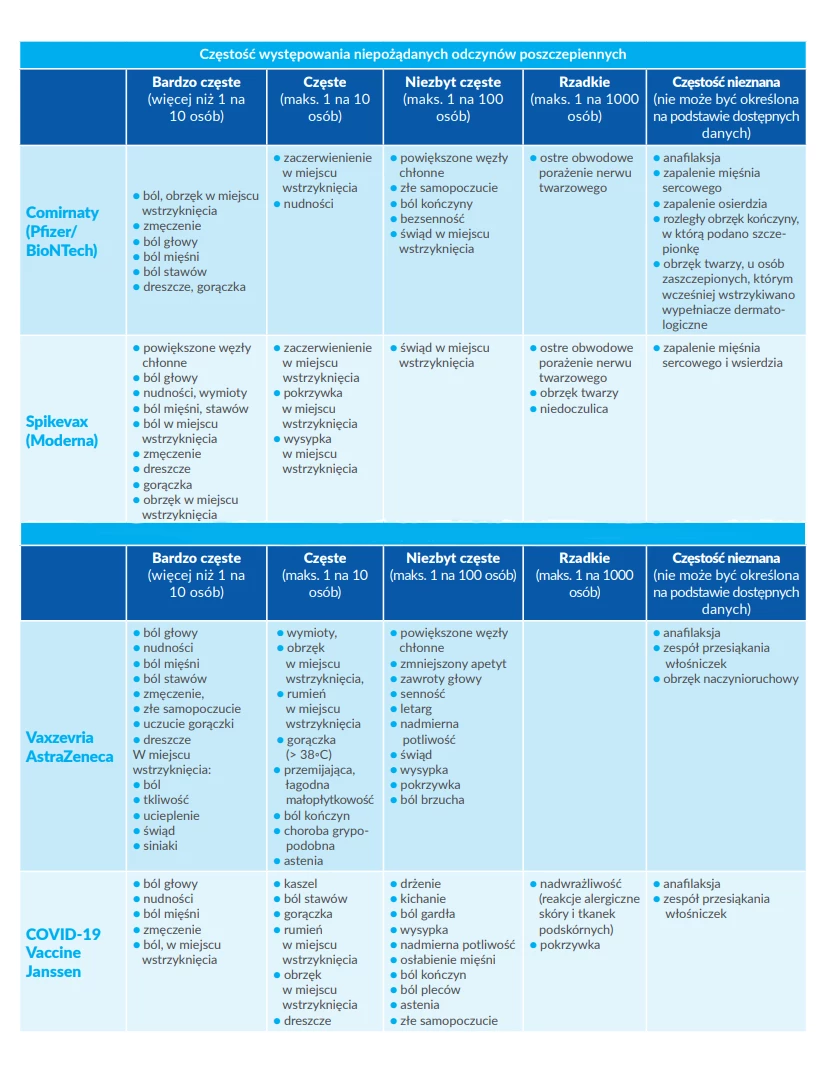
- Jakie szczepionki na COVID-19 są dostępne na rynku?
- COVID-19 - gdzie i jak się zaszczepić?
- Jak przygotować się do szczepienia na koronawirusa?
- Czy szczepionka na COVID-19 jest płatna?
- Czy szczepienie na koronawirusa jest obowiązkowe?
- Co powinniśmy wiedzieć na temat szczepienia na COVID-19?
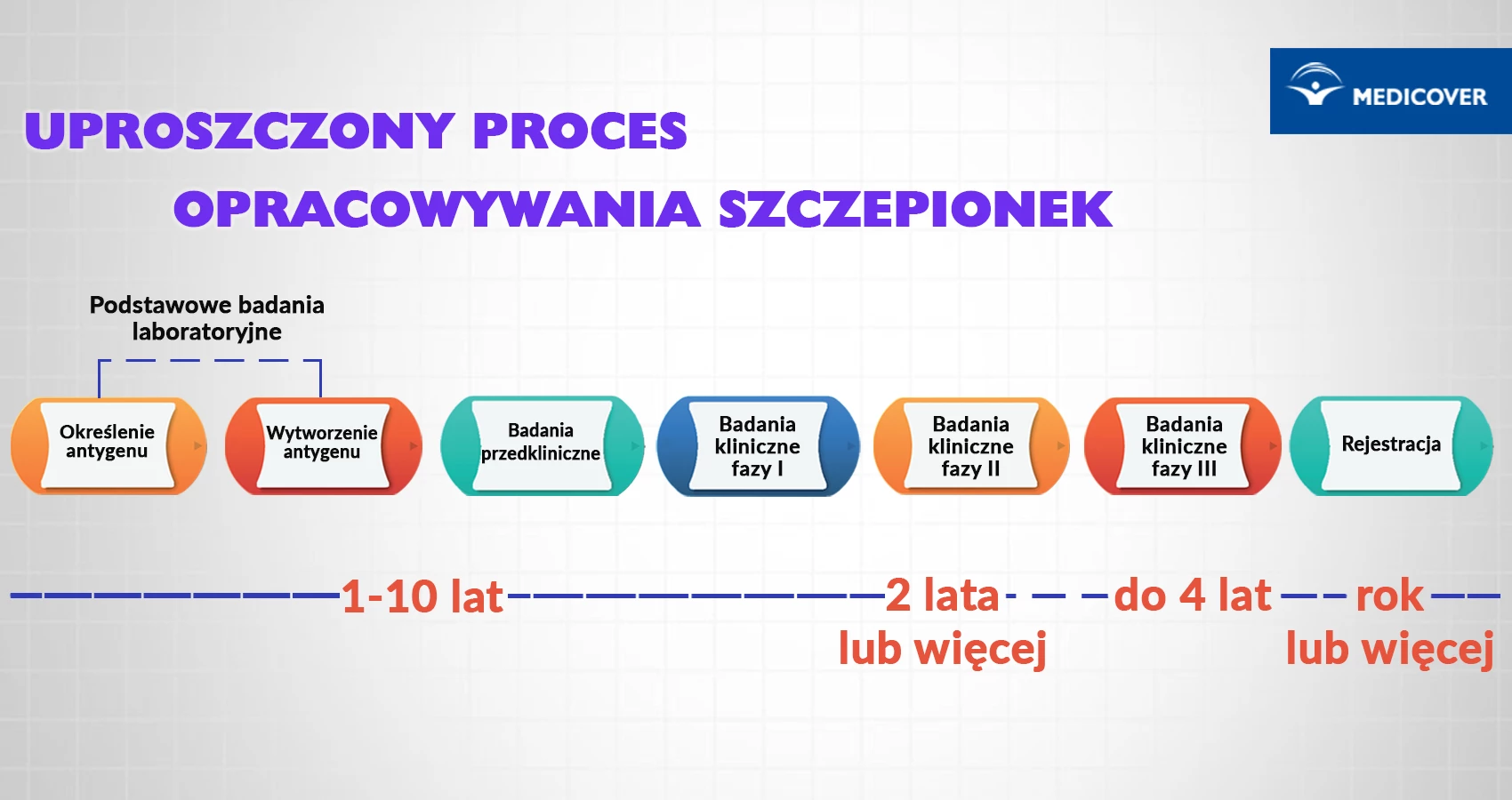
- Etapy powstawania szczepionki
 Szczepienia COVID-19. Najczęstsze pytania i odpowiedzi
Szczepienia COVID-19. Najczęstsze pytania i odpowiedzi
Szczepienia dawką przypominającą - SPRAWDŹ INFORMACJE >>
Szczepienia przeciwko COVID-19
Od początku pandemii badacze z całego świata intensywnie pracowali nad stworzeniem szczepionki. Wiele osób obawiało się, że tempo powstania szczepionki na COVID-19 było zbyt szybkie, aby dokładnie ocenić jej bezpieczeństwo i skuteczność.
Wiele prac, badawczych i legislacyjnych, prowadzono jednocześnie, a agencje odpowiedzialne za dopuszczanie leków na rynek (jak europejska EMA czy amerykańskie FDA) pozwalały na dostarczanie dokumentów partiami. Ponadto skrócono wiele urzędowych terminów potrzebnych do złożenia odpowiednich dokumentów czy wydania opinii. Jednak mimo pewnych przyspieszeń, nie zrezygnowano ze standardowych procedur związanych z jakością, bezpieczeństwem i skutecznością szczepionki – te same fazy badań klinicznych i procedury co przy standardowej szczepionce zostały przeprowadzone w krótszym czasie. Więcej dowiesz się na: https://www.ema.europa.eu/en/human-regulatory/overview/public-health-threats/coronavirus-disease-covid-19/treatments-vaccines/covid-19-vaccines-development-evaluation-approval-monitoring.
Po przeprowadzeniu badań klinicznych szczepionka musi zostać zatwierdzona przed odpowiednie instytucje (np. EMA, FDA) przed wprowadzeniem jej do obrotu.
Sprawdź: Nowa fala zakażeń COVID-19 w 2025. Dominujące objawy i zalecenia
Szczepionka na COVID-19 - kolejna dawka przypominająca
Minister Zdrowia zaleca przyjęcie szczepionki zaktualizowanej pod aktualnie dominujący podwariant XBB.1.5. Możliwość wykonania szczepienia zostanie uruchomiona od 6 grudnia 2023 r.
Szczepienie zaleca się:
- osobom w wieku powyżej 60 lat;
- osobom z niedoborami odporności lub chorobami współistniejącymi, zwiększającymi ryzyko ciężkiego przebiegu COVID-19 (dotyczy osób w wieku powyżej 12 lat);
- pracownikom ochrony zdrowia, którzy mają bezpośredni kontakt z pacjentem lub materiałem zakaźnym.
Gdzie się zaszczepić?
Zgodnie z komunikatem nr 34 Ministra Zdrowia w sprawie realizacji szczepień przeciw COVID-19 w sezonie 2023/2024 podmiotami uprawnionymi do wykonywania szczepień przeciw COVID od 1 grudnia 2023 r. będą wyłącznie:
- przychodnie POZ,
- apteki ogólnodostępne.
W konsekwencji tych zmian szczepienia przeciwko COVID-19 nie będą możliwe do realizacji w Centrach Medycznych Medicover.
Aktualna lista placówek wykonujących szczepienia od 1 grudnia 2023 r. znajduje się tutaj:
Mapa punktów szczepień - Szczepienie przeciwko COVID-19 - Portal Gov.pl
Szczepionka z wariantem XBB (Kraken) – co warto o niej wiedzieć?
Szczepionka białkowa podjednostkowa Nuvaxovid (firmy Novavax) jest zaktualizowana pod aktualnie dominujący podwariant XBB.1.5. i będzie dostępna również dla osób, które wyrażają chęć zaszczepienia i spełniają warunek wieku (osoby, które ukończyły 12 r.ż.), a od ostatniego szczepienia przeciwko COVID-19 upłynęło co najmniej 6 miesięcy.
W przypadku osób powyżej 12. roku życia dotychczas nieszczepionych przeciw COVID-19 należy podać 2 dawki w odstępie 3 tygodni.
Zalecany odstęp podania kolejnej dawki przypominającej od przyjęcia ostatniej dawki przypominającej w grupie wiekowej 12+ wynosi co najmniej 6 miesięcy.
Pełna treść komunikatu Ministra Zdrowia w sprawie realizacji szczepień przeciw COVID-19 w sezonie 2023/2024: Komunikat nr 34 Ministra Zdrowia w sprawie realizacji szczepień przeciw COVID-19 w sezonie 2023/2024 – Ministerstwo Zdrowia - Portal Gov.pl
Szczepionka przeciwko COVID-19 - materiały do pobrania przed szczepieniem
Kwestionariusz wstępnego wywiadu przesiewowego przed szczepieniem osoby dorosłej przeciw COVID-19:
Wersja polska (Pobierz plik PDF >>)
Wersja polsko-angielska (Pobierz plik PDF >>)
Wersja polsko-rosyjska (Pobierz plik PDF>>)
Wersja ukraińska (Pobierz plik PDF >>)
Kwestionariusz wstępnego wywiadu przesiewowego przed szczepieniem osoby niepełnoletniej (12-17 lat):
Wersja polska (Pobierz plik PDF >>)
Wersja angielska (Pobierz plik PDF >>)
Wersja rosyjska (Pobierz plik PDF>>)
Wersja polsko-ukraińska (Pobierz plik PDF >>)
Kwestionariusz wstępnego wywiadu przesiewowego przed szczepieniem dzieci (5-11 lat):
Wersja polska (Pobierz plik PDF >>)
Wersja angielska (Pobierz plik PDF >>)
Wersja rosyjska (Pobierz plik PDF >>)
Wersja polsko-ukraińska (Pobierz plik PDF >>)
Kwestionariusz wstępnego wywiadu przesiewowego przed szczepieniem dzieci i noworodków (6 miesięcy-4 lata):
Wersja polska (Pobierz plik PDF >>)
Wersja angielska (Pobierz plik PDF>>)
Wersja rosyjska (Pobierz plik PDF>>)
Wersja polsko-ukraińska (Pobierz plik PDF>>)

 Medicover
Medicover